
Endokrinológus
A Budai Endokrinközpont specialistája "endokrinológia" témakörben
Kérem, tegye fel kérdéseit, készséggel válaszolok Önnek! Bizalmát köszönöm!
Témakörök ►
Kérdezz-felelek
Tisztelt Professzor úr!
Évek óta gyermeket szeretnék, de vélhetően a nagyon magas antiTPO szintem ezt megakadályozza( diagnosztizált Hashimoto, aTPO >3000 ). Ez az érték folyamatos Euthyrox kontroll illetve 200mcg szelén szedése mellett sem akar lentebb menni. Nagyon részletes immunológiai és belgyógyászati kivizsgálásokon estem túl, úgy tűnik az okokat felderítettük, feltételezhetően a túl magas antiTPO szintre vezethető vissza, hogy többször sikertelen lett az IUI, és a baba nem tud megtapadni.
A kérdésem az Intralipid terápiára vonatkozik, ebben kérném szíves véleményét kikérni.
Az interneten kutakodva azt olvastam, hogy az USAban sikerrel alkalmazzák az Intralipid kezelést olyan nők esetében, ahol immunológiai okok feltételezhetőek a sikertelen IVF, IUI kezelések hátterében. Ilyen pl a magas NK-Cell aktrivitás vagy a magas antiTPO. Rengeteg sorstárs számol be sikerről, hogy a korábban sikertelen IVF-ek után, a következő IVF kezelés előtt beadott Intralipid terápia sikeres megtapadáshoz vezetett!
Azt szeretném kérdezni Öntől, hogy Magyarországon el lehet-e indulni ilyen irányú kivizsgálások felé, lehet-e ilyen terápiát kérni? Egyáltalán az Intralipid infúzió van-e törzskönyvezve ilyen célra, lehetséges-e a beadása ebből a célból?
Érdeklődöm, hogy egy személyes konzultáció keretében tud-e ezekre választ adni, érdemes -e ebben a lehetőségben gondolkodni?
Felcsillant a remény, hogy talán ezen az úton elindulva nem kellene végleg lemondanom a gyermekáldás lehetőségéről. Sajnos az elmúlt 6 évben nem sikerült az antiTPO szintet letornászni és minden eddigi próbálkozás eredménytelen maradt. De bízom benne, hogy ez az út talán még járható.
Jó egészséget kívánok Önnek!
Beáta
Tisztelt Beáta!
Itthon az Intralipid infúzió elérhető, azonban alkalmazása off-label, tehát nem engedélyezett ezen indikáció alapján, hasonlóan a IVIG terápiához. Egyébként - mivel kérdéésből kiderül, hogy tájékozott a témában - fontos megemlítenem, hogy a kezelés során az anti-TPO antitestek funkciója nem azonos, tehát van toxikus, az enzim működését gázló és protektiv hatású is. Ez azt jelzi, hogy az anti-TPO teljes mennyisége jelzi a betegállapotát. Ezért kicsit részletesebben válaszolok:
A legújabb európai populációban végzett vizsgálatok azt mutatták, hogy a pajzsmirigy betegségei népbetegségnek számítanak, mivel a teljes lakosságban a hypothyreosis 4,4%-ban, a hyperthyreosis 1,4%-ban fordul elő. A hypothyreosis a lakosság 0,4%-ban manifeszt, 4,0%-ban enyhe, ill. szubklinikus formában mutatható ki . Az Amerikai Egyesült Államokban az u.n. NHANES III („Third National Health and Nutrition Examination Survey), hasonló statisztikai adatokat mutatott. A hypothyreosist a lakosság 4,6%-ban, a hyperthyreosist 1,3%-ban bizonyították. Az átlagosnál magasabb jódbevitel a golyvák alacsonyabb, de a hypothyreosis magasabb incidenciájával mutatott összefüggést, az átlagosnál alacsonyabb jódfogyasztás viszont növelte a toxikus göbös golyva és ezzel együtt a hyperthyreosis prevalenciáját. Az idiopathiásnak tartott hypothyreosisos betegek többségében autoimmun eredetet tudtak igazolni. Az autoimmun thyreoiditisek (AT-k) gyakran szubklinikus formában jelennek meg, ezért a betegség gyakoriságáról nehéz pontos adatokat szerezni. Nőkben a betegség lényegesen gyakoribb, mint férfiakban (4-5:1). A betegség korai felismerése azért is fontos, mert szubklinikus formában is jelentős rizikófaktora számos betegségnek, így a korai vetélésnek és a meddőségnek. Az AT lefolyásában négy stádiumot különíthetünk el: l Hyperfunkciós stádium: betegség kezdetétől számított 1-6 hét. A tünetek az acinussejtek károsodása miatt felszabaduló jelentős mennyiségű hormon következtében jönnek létre („destruktív hyperthyreosis”). 2. Hypofunkciós stádium: a betegség kezdetétől számított 8. héttől 4-6 hónapig. 3. Regenerációs stádium: A betegség kezdetétől számított 7-12 hónap. 4. Definitív stádium: ha a regeneráció teljes, akkor a beteg gyógyult, míg a betegek többségében súlyos, enyhe, esetleg szubklinikus hypothyreosis alakul ki. A hypothyreosis egyes formáinak meghatározásában alapvető az élettani TSH szint definíciója. A szuperszenzitiv TSH (sTSH) módszerek lehetővé tették a szubklinikus és az enyhe hypothyreosis megkülönböztetését. A sTSH 2.5 mU/l felső szintjét az irodalom általában elfogadja, de számos, a szerzők által is leírt megkötést is megfogalmaz. A fiziológiás TSH szint felső határának 4,5-ről 2,5 mU/l-re csökkentése azt is eredményezte, hogy az Egyesült Államokban a szubklinikus hypothyreosisos betegek száma meghaladja a 20 milliót. Módszertani szempontból fontos, hogy a TSH szint meghatározása immunológiai metodikával történik, ami azt jelenti, hogy az un. „immunreaktív” TSH-t és nem a biológiailag aktív TSH szintet határozzuk meg. Célszerű volna az immunológiai és biológiai TSH szint hányadosát (I/B) mérnünk, ez azonban egyelőre anyagi okok miatt a mindennapok diagnosztikájában még nem lehetséges. Tovább bonyolítja a helyzetet, hogy a betegek savójának egy részében TSH-t megkötő faktorokat (antitesteket, szolubilis receptorokat) lehet kimutatni. Az AT patomechanizmusában fontos szerepe van a thyreoglobulin(Tg) és a peroxidáz enzim (TPO) elleni antitesteknek. A TPO elleni antitestek az egészséges férfiak 8,6%-ban, a nők 18,5%-ban bizonyultak pozitívnak. A TPO elleni antitestek poliklonálisak és egy részük képes direkt citotoxikus módon károsítani a pajzsmirigyet, más részük pedig a TPO enzim működését gátolja 3,4,5,15,19. Az IgG típusú TPO elleni antitestek kimutathatók a köldökzsinórvérben és átjutnak a magzatba is. Ebből a szempontból is érdekes, hogy azokban a gyermekekben, akiknek köldökzsinórvérében a TPO elleni antitestek kimutathatóak voltak, az AT kialakulása is szignifikánsan gyakoribbnak bizonyult22. Bizonyították a TPO elleni antitestek szerepét meddőségben, ugyanis a terméketlen nőkben a TPO elleni antitest 31.8%-ban, a fertilis, egészséges populációban csak 4.6%-ban volt kimutatható. A TPO elleni antitest pozitívakban akkor is szignifikánsan nagyobb volt az infertilisek aránya, ha a hormon értékeik (hypophysis és perifériás hormonok) élettani tartományban voltak. A TPO elleni antitesteknek fontos szerepe van a vetélésekben is, ugyanis TPO elleni antitest pozitívakban a spontán vetélések száma jelentősen magasabb, mint az antitest negatívakban (32% v.s. 6%). A 3-szor vagy több alkalommal vetéltek között pedig a magas TPO elleni antitest titerűek száma kétszer nagyobbnak adódott. A TPO elleni antitesteknek jelentőségük van a magzati fejlődésben is. A magzat fizikai fejlődése (érése) 19,3%-ban gátolt a TPO elleni antitest pozitív anyákban, a szellemi fejlődés, az IQ érték 10,5 ponttal alacsonyabb a TPO elleni antitest jelenlétében4,5,11.
Az alábbiakban a következő kérdésekre igyekszünk választ adni:
I. Milyen immunológiai mechanizmusok biztosítják a magzat megtapadását és fejlődését?
II. Mi a kapcsolat az autoimmun pajzsmirigybetegség és a meddőség, a spontán vetélések között?
III. Melyek a legújabb diagnosztikus és terápiás ajánlások?
Ad I. Milyen immunológiai mechanizmusok biztosítják a magzat megtapadását és fejlődését?
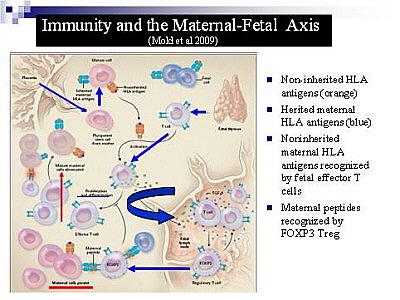
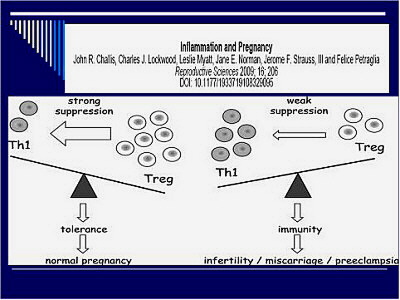
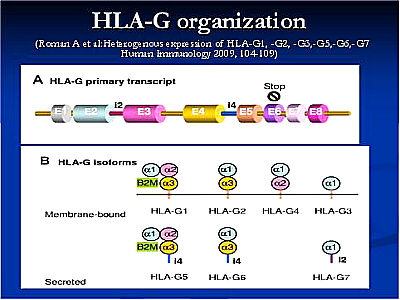
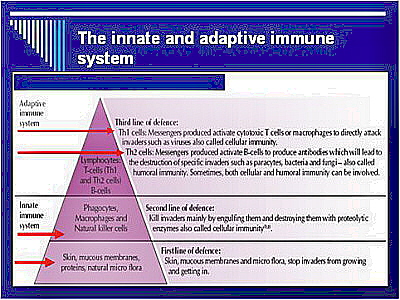
Az endokrinológia, immunológia és a genomika módszereinek alkalmazása forradalmi változásokat eredményeztt a terhességgel kapcsolatos kutatásokban. Az un. microarray technika lehetőséget nyújt a cytokin termeléssel és növekedéssel kapcsolatos génexpressziós mechanizmusok tanulmányozására. A magzat fiziológiás transzplantátum, amelynek kilökődését számos védő mechanizmus akadályozza. A terhesség alatt a T helper-2 (Th2)(humorális immunitásért felelős) cytokinek mennyisége növekszik a T helper1 (Th1) (celluláris immunitásért felelős) által termelt citokinekkel szemben. Ennek következtében a Th1 által közvetített immun- és autoimmun folyamatok aktivitása általában csökken, ezért élettani körülmények között a terhesség 2.-ik trimeszterétől kezdve az autoimmun betegségek tünetei általában javulnak . Amennyiben ez a fiziológiás immunszuppresszió nem alakul ki, akkor kóros terhesség és spontán abortusz következhet be . A Th1 cytokinek tehát a terhesség kimenetele szempontjából kedvezőtlen hatásúak. A Th1 csoportba tartozó gamma interferon (INFγ) cytotoxikus T sejteket aktivál, amelyek károsíthatják a magzatot. Az INFγ gátolja a trofoblaszt növekedését, illetve a Th2 cytokineket produkáló sejtek szaporodását és ennek révén az immunglobulinok termelését is. A másik Th1 cytokin, a TNFα közötti kapcsolat is ismert. Egerekben a TNFα-val történő kezelés a terhesség megszakadásához vezetett. A TNFα szint emelkedését figyelték meg a habituálisan vetélő nőkben is. A Th1 cytokinek termelését indukáló vírusfertőzésekről ismert, hogy szerepük van a spontán abortuszok kiváltásában,20. Az élettani terhességben fontos, hogy az anya lymphocytái felismerjék a magzati antigéneket, tehát az immuntolerancia egy aktív immunreguláció eredménye. Az egyén immunológiai ujjlenyomatának tekinthető HLA antigének teszik lehetővé, hogy az immunrendszer a saját és az idegen struktúrákat megkülönböztesse. A trofoblasztokról hiányoznak a polimorf HLA antigének, de a szervezetben gyakorlatilag egyedülállóan expressszálódnak a HLA-G molekulák. Ezek a MHC I. osztály molekuláitól eltérően alacsony polimorfizmust mutatnak. A HLA-G molekulák expresszálódnak a placentán, a thymuson, azonban az MHC I osztály további antigénjei (HLA–A és B) nem mutathatók ki (2. ábra). A HLA-G gén szerkezete hasonló a többi I. osztályú HLA gének szerkezetéhez, de sajátos promoter regióval rendelkezik és a transzkriptumok (mRNS) változatos hasítása („splicing”) következtében több membránhoz kötött és/vagy szolubilis izoformát produkálnak (3.ábra). A szolubilis HLA-G kulcsfontosságú a terhesség megtartása szempontjából, mivel azok az embriók implantálódnak sikeresen, amelyek aktívan képesek a HLA-G molekulákat szecernálni. A HLA-G expresszióban megfigyelhető különbségek részben genetikailag determináltak. A HLA-G kódoló gén 8. exonjának 3’- nem transzlálódó régiójában található egy 14 bp hosszú szakasz, amelynek deléciója vagy inszerciója összefüggésébe hozható a mesterséges megtermékenyítés sikertelenségével és a habituális vetélés fokozott kockázatával. Ennek a 14 bp hosszúságú szakasznak meghatározó fontossága van az immunmoduláció létrejöttében, az anyai gyilkos („killer”) sejtek átmeneti „megvakításában”. Érdekes, hogy a habituálisan vetélő nők férjeinek jelentős részében a HLA-G alléleken hiányzik ez a 14 bp hosszúságú szakasz, míg feleségeik döntő többségében ezt a 14 bp szekvenciát tartalmazó homozigóta HLA-G allélek kimutathatók10,14,17,18.
Ad II. Mi a kapcsolat az autoimmun pajzsmirigybetegség és a meddőség, a spontán vetélések között?
A pajzsmirigy autoimmun betegségei és a terhesség közötti kapcsolatra több magyarázat van.
o A vetélés kapcsolatban lehet azzal az egyensúlyzavarral, amely az autoimmun betegség alatt a Th1 és a Th2 arány kedvezőtlen változásával függ össze. További rizikófaktort jelenthet, ha az anyának korábban fiú gyermeke volt. A magzati eredetű sejtek ugyanis beépülnek a pajzsmirigybe és több évtizeddel a szülést követően is kimutathatók és un. mikrokimerizmust hoznak létre. Ez a „host versus graft” reakció sajátos formája és magyarázatot ad arra megfigyelésre, hogy azokban az anyákban, akik korábban fiú gyermeket szültek, az autoimmun pajzsmirigybetegség többször fordul elő.
o Az autoimmun pajzsmirigybetegségben szenvedőkben a pajzsmirigyhormonok viszonylagos, ill. abszolút hiánya figyelhető meg. Glinoer és mtsai az első trimeszterben minimálisan emelkedett TSH-t mutattak ki. Amennyiben a TSH érték 2,5 mU/l fölé emelkedett és a TPO elleni antitest szintjük is magas volt, akkor a vetélés kockázata lényegesen növekedett. Jóllehet ez a megfigyelés nem ad magyarázatot a thyreoiditis és a magzati rendellenességek közötti közvetlen összefüggésre, azt azonban jelzi, hogy az immunrendszer aktiválódása (antitest titer emelkedése) és a csökkent pajzsmirigy aktivitás mindenképpen káros a magzat szempontjából.
o A harmadik hipotézis az anyai életkorral magyarázza a jelenséget. Az autoimmun pajzsmirigybetegségben szenvedők átlagos életkora magasabb, mint az egészségeseké, az emelkedett kor tehát önmagában felelős lehet a fokozott vetélési hajlamért.
Ad III. Melyek a legújabb diagnosztikus és terápiás ajánlások?
A nemzetközi irodalomban egyértelmű állásfoglalás található arra, hogy a terhesség, sőt a fogantatás előtt a szubklinikus és a manifeszt hypothyreosist el kell kerülnünk megfelelő szubstituciós kezeléssel. A hypothyreosis kezelése azonban nem egyszerű feladat, mivel kicsiny az un „terápiás ablak”, azaz nem könnyű megtalálni az ideális dózist és készítményt. A gyakori TSH meghatározások azért sem javasolhatók, mert a thyroxin (T4) dózis változtatását a TSH szint csak megkésve követi. Az a tény, hogy az egyes T4 készítmények biológiai hasznosulása („bioviability”) lényegesen eltér egymástól, további óvatosságra inti a kezelést elindító, ill. ellenőrző szakorvost. Általános elvként leszögezhető, hogy a T4 kezelést alacsonyabb dózissal kell elkezdeni még akkor is, ha kísérő betegségek (pl. súlyos szívbetegségek) nincsenek. Az 1,0 körüli TSH érték elérése mellett az egyedi kezelés során, az életminőség javulását kell szem előtt tartani. A T4 kezelés hatására önmagában is csökken az autoantitestek titere és mérséklődik a pajzsmirigy állományának pusztulása. Ez a klinikai megfigyelés azzal az experimentális adattal magyarázható, hogy a T4 csökkenti a TSH szintet, mely képes a thyreocyták HLA-DR expressziójának növelésére ("izohormonális" kezelés). A legújabb kutatások azt bizonyították, hogy a szelén lényeges szerepet játszik a pajzsmirigy működésében. Két fő hatása van: l. Befolyásolja a mirigy hormonjainak képződését és le bontását, mivel a szelén tartalmú enzimek (dejodinázok) döntőek a thyroxinnak (T4) trijódthyroninná (T3) történő konverziójában, tehát az aktív metabolit képzésében. 2.A pajzsmirigyben a hormonképzés során magas a szabad oxigén-gyökök szintje és a szelén, ill. a szelenoproteinek jelentős gyökfogó hatásuk miatt védik a szöveteket. Az pajzsmirigybetegségben szenvedő infertilis nőkben gyakran figyeltek meg a szelén kezelés után gyermekáldást . A leggyakoribb diagnosztikus kérdés az, hogy a TPO elleni antitestek meghatározását minden terhes számára javasoljuk-e? A nemzetközi álláspont szerint a rutinszerű antitest meghatározás egyelőre nem javasolt, ha azonban fertilitási zavar, spontán abortuszok voltak, akkor előzetes endokrin konzílium után elvégzése tanácsos . Ezzel kapcsolatban irányelvként elfogadhatjuk az Amerikai Pajzsmirigy Társaság 2009-es ajánlását . A terhesség alatt kialakuló védő faktorok eredményeképpen az autoantitestek titere a terhesség alatt általában csökken, a szülést követően viszont emelkedik. Amennyiben ez a fiziológiás védő mechanizmus sérül (genetikai és környezeti faktorok miatt), akkor a szülést követő 3-12 hónap múlva post-partum thyreoiditis (PPT) alakulhat ki a szülések 3-17 %-ban. A PPT népegészségügyi jelentőségét az adja, hogy ez a betegség a hypothyreosis egyik leggyakoribb oka, korai felismerése azért is fontos, mert szubklinikus formában is jelentős rizikófaktora lehet menstruációs és fertilitási zavaroknak, spontán abortuszoknak, az újszülöttek mentális retardációjának, az anya ischemiás szívbetegségeinek. A fentiek arra hívják fel a figyelmet, hogy a fertilis korban lévő, pajzsmirigybetegségben szenvedő nők gondozása szükséges.
A jobb áttekinthetőség kedvéért néhány ábrát is csatolok.
Balázs Cs, Farid NR: Soluble CD4 concentrations predict relapse of post-partum thyroiditis. J.Endocrinol.Invest. 2002; 25: 11-17.
Carosella ED, Favier B, Rouas-Freiss N, Moreau P, LeMaoult J: Beyond the increasing complexitiy of the immunomodulatory HLA-G molecule. Blood 2008,; 111: 4862-4868.
Guerin LR, Prins JR, Robertson SA: Regulatory T cells and immune tolerance in pregnancy: a new target for infertility treatment? Human Reproduction Update 2009; 1: 1-19.
Kaczur V, Vereb Gy, Molnár I. és mtsai: Effect of anti-thyroid peroxidase antibodies on thyroid peroxidase activity measured by chemiluminescence technique.Clin. Chem. 1997; 43: 8-14
Kuroki K, Maenaka K: Immune modulation of HLA-G dimer in maternal-fetal interface. Eur J Immunol 2007; 37: 1727-1729.

Jó egészséget kívánok:
Prof. Dr. Balázs Csaba
2012-03-07 07:45:40











